审评改革浪潮下的技术转让 机遇与挑战并存
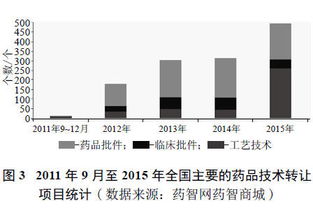
中国药品审评审批制度的改革步伐不断加快,一系列旨在鼓励创新、提升药品质量、加速新药上市的政策相继出台。这场深刻的变革,不仅重塑了药品研发与上市的格局,也为药品技术转让这一传统业务领域带来了前所未有的机遇与严峻的挑战。技术转让作为链接研发与生产、优化资源配置的重要环节,正处于一个关键的转型路口。
机遇:审评改革催生技术转让新蓝海
- 政策东风,鼓励资源流动:审评制度的优化,特别是《药品管理法》的修订及配套法规的实施,明确了技术转让的合法路径和简化程序。对于已获批的药品,技术转让的审评时限有望缩短,降低了交易的时间成本和不确定性,为存量药品的技术转移注入活力。
- 创新驱动,转让标的升级:随着以临床价值为导向的审评标准确立,以及药品上市许可持有人(MAH)制度的全面推行,创新药和改良型新药成为研发热点。这催生了大量早期研发项目、专利技术乃至已进入临床阶段的优质资产寻求合作与转让,技术转让的标的从传统的仿制药文号,向更具技术含量和市场潜力的创新资产延伸。
- 专业分工,生态合作深化:MAH制度实现了药品上市许可与生产许可的“解绑”,使得研发机构、科研人员可以专注于创新,而将生产委托给具备条件的生产企业。这极大地促进了产业链的专业化分工,技术转让不再仅仅是文号的简单买卖,而是演变为涵盖研发、临床、生产、销售全链条的深度战略合作,形式更加灵活多样。
- 市场扩容,价值重估:审评加速使得药品生命周期管理的重要性凸显。对于持有文号但缺乏市场推广能力的企业,通过技术转让引入有实力的合作方,可以快速实现产品价值。随着中国医药市场持续增长和对优质药品需求的提升,具有临床优势的药品技术价值也水涨船高。
挑战:新规之下技术转让的复杂考验
- 法规与技术要求趋严:审评改革在提速的对药品全生命周期的质量管理提出了更高要求。技术转让不再仅仅是资料和批件的转移,更涉及生产工艺、质量控制体系的完整转移和验证。受让方必须具备相应的生产条件和质量管理能力,并确保转移前后产品质量的一致性。这显著提高了技术转让的技术门槛和合规成本。
- 价值评估与定价难题:对于创新性技术资产,其价值评估变得更为复杂。如何科学评估尚在早期研发阶段项目的临床前景、专利壁垒和市场潜力,成为交易双方的核心难点。定价机制的不成熟可能导致交易失败或价值扭曲。
- 过程复杂性与风险增加:技术转让是一个系统工程,涉及技术资料转移、工艺验证、稳定性研究、注册申报等多个环节。在MAH制度下,还涉及持有人变更、委托生产协议、质量责任界定等法律与商业安排。任何环节的疏漏都可能导致审评延误或注册失败,风险贯穿全程。
- 市场竞争与信息不对称:随着市场活跃度提升,优质技术资产竞争加剧。转让方与受让方之间在技术细节、研发数据、市场判断等方面可能存在信息不对称,增加了交易的谈判难度和后续整合风险。
应对之道:在变革中把握主动
面对机遇与挑战,相关企业需积极调整策略:
- 提升专业能力:无论是转让方还是受让方,都必须深入理解最新法规,建立强大的技术评估、项目管理与合规体系。
- 强化尽职调查:进行全方位、深度的技术、法律、财务及市场尽职调查,是规避风险、达成公平交易的基础。
- 创新合作模式:探索分期付款、里程金、销售分成、股权合作等灵活的交易结构,以平衡风险与收益。
- 依托专业平台:积极利用行业协会、专业咨询机构及交易服务平台,获取信息、撮合交易、规范流程。
中国药品审评制度改革为技术转让开辟了更广阔的空间,但也设定了更高的标准。唯有那些能够精准识别价值、高效执行转移、严守质量底线的参与者,才能在这股浪潮中乘风破浪,实现技术与市场的成功对接,最终惠及患者,推动中国医药产业的高质量发展。
如若转载,请注明出处:http://www.kzlhn.com/product/28.html
更新时间:2026-05-30 05:17:22